هنگامی که باتری آتش میگیرد، اغلب توجهها متوجهی کارخانهی سازنده است. چرا که در آزمایشات پیشتولید خود موفق به آشکارسازی چنین مشکلی نشده است. اینطور مشکلات باتریها را میتوان به حساب شرکتهایی گذاشت که آخرین تکنولوژیها مرزی را در محصولاتشان به کار میگیرند. به عنوان مثال هرچه صفحهی نمایش بزرگتر و گوشی از نظر پردازشی قدرتمندتر گردد، نیاز به انرژی بیشتری دارد، اما تولیدکنندگان هر طور که شده این فشار را برروی باتریها با فناوری موجود میآورند تا پاسخگوی نیاز کاربران باشد. بخواهیم صادقانه بگوییم، شاید کاربری نباشد که بخواهد از ظرفیت باتری و سرعت شارژ شدن بالا بگذرد.
طبق گفتهی دانشمندان علوم مواد شناسی دانشگاه کُرنل، هماکنون به ۹۰ درصد ماکزیمم ظرفیت تئوری باتریهای یون لیتیوم رسیدهایم. بنابراین سازندگان تنها روی مقدار محدودی از انرژی در حال مانور دادن هستند و میخواهند ظرفیت باتری خود را بیشتر از رقبا کنند. کاری که بین تولیدکنندگان در حال باب شدن است.
طبق گفتهی دانشمندان علوم مواد شناسی دانشگاه کُرنل، هماکنون به ۹۰ درصد ماکزیمم ظرفیت تئوری باتریهای یون لیتیوم رسیدهایم. بنابراین سازندگان تنها روی مقدار محدودی از انرژی در حال مانور دادن هستند و میخواهند ظرفیت باتری خود را بیشتر از رقبا کنند. کاری که بین تولیدکنندگان در حال باب شدن است.

سامسونگ در این فراخوانی سراسری ادعا میکند در کمتر از ۰.۱درصد از دستگاهها، اتصالکوتاهی در داخل باتری رخ داده است. اما دلایل بسیار مرسوم دیگری میتوان برای باتریهای یونلیتیوم ذکر کرد. و همانطور که گفتیم، این احتراق معمولا هنگامی که بیش از اندازه بخواهیم از باتری توان بکشیم، رخ خواهد داد. دلیل آنکه مهندسین از لیتیوم جهت ساخت در باتریها استفاده میکنند، به دلیل وزن کم آن و توانایی ذخیرهسازی مقدار زیادی از انرژی است.
سامسونگ تلاش کرده بود تا یک هفته قبل از معرفی iPhone 7، موج گوشیهای هوشمند را در دست بگیرد اما با چنین رخدادی، به نظر میرسد این هدف تا اندازهای محقق نشده باشد.
برای آنکه بدانیم چه المانهایی یک باتری را امن میکند، باید شیوهی کار آن را جویا شویم. همهی ما از دوران مدرسه به یاد داریم که دو نوع الکترود و یا رسانای الکتریکی داریم که در دو سمت قطب قرار گرفتهاند. الکترودی که یونهای شارژ شدهی مثبت را نگهداری میکند، کاتد نام دارد. کاتد از لیتیوم پر شده است و جایی است که سوخت(انرژی) در آن ذخیره شده است. در مقابل، جایی که الکترودهای یونهای منفی قرار دارند، آند نام دارد.
سامسونگ تلاش کرده بود تا یک هفته قبل از معرفی iPhone 7، موج گوشیهای هوشمند را در دست بگیرد اما با چنین رخدادی، به نظر میرسد این هدف تا اندازهای محقق نشده باشد.
برای آنکه بدانیم چه المانهایی یک باتری را امن میکند، باید شیوهی کار آن را جویا شویم. همهی ما از دوران مدرسه به یاد داریم که دو نوع الکترود و یا رسانای الکتریکی داریم که در دو سمت قطب قرار گرفتهاند. الکترودی که یونهای شارژ شدهی مثبت را نگهداری میکند، کاتد نام دارد. کاتد از لیتیوم پر شده است و جایی است که سوخت(انرژی) در آن ذخیره شده است. در مقابل، جایی که الکترودهای یونهای منفی قرار دارند، آند نام دارد.
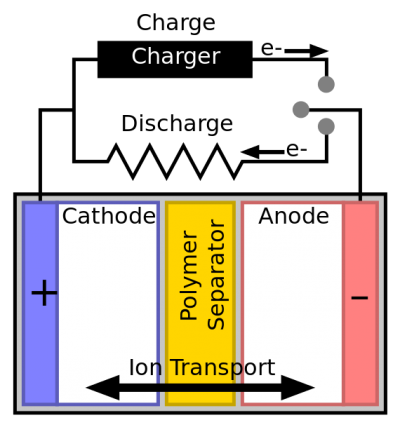
در هنگام شارژ، یونهای لیتیوم از کاتد به آند حرکت میکنند. هنگام استفاده از باتری، این مسیر در لیتیوم برعکس میشود. در این بین مواد شیمیایی به نام الکترولیتها وجود دارند که حرکت یونها را راحتتر میکنند. اگرچه یونها میتوانند از آند به کاتد و برعکس حرکت کنند، اما برای کاتد و آند نباید چنین اتفاقی بیفتد، به دلیل آنکه انرژی را به سمت الکترولیتها بر میگرداند. برای جلوگیری از چنین واقعهای، سازندگان باتری از جداکنندهها استفاده میکنند.
برای Galaxy Note 7 نیز چنین اتفاقی افتاده بود. جداکنندهها خراب شده بودند و الکترودها به یکدیگر متصل شده بودند. برای باتری این بدترین اتفاق است، چرا که منجر به انفجار و آتشسوزی میگردد. هنگامی که التکرودها به هم تماس پیدا میکنند، تمامی انرژیها به جای آنکه به دو سمت(قطب) باتری سرازیر شوند، به مرکز باتری که الکترولیتها قرار دارند، میروند.
الکترولیتها خیلی پایدار نیستند و در اثر کوچکترین تغییراتی از حالت ایمن خارج میشوند. هنگامی که گرمای زیاد، چه به دلیل گرمای بیرونی و چه اتصال کوتاه، ایجاد میشود، میتواند الکترولیتها را به واکنش با دیگر مواد شیمیایی و تولید گازهایی وادار کند که همین تولید گاز منجر به گرمای بیشتری گردد. هر بار که این مواد شیمیایی با یکدیگر واکنش انجام میدهند، گازهای بیشتری با سرعت بالاتری تولید میکنند. این کار باعث ورود به حلقهای به نام «گریز گرما» میگردد که نهایتا چیزی جزء آتشسوزی و انفجار نیست. به همین دلیل است که هنگامی که گوشی موبایل بیش از اندازه داغ شد، دستگاه به طور خودکار خاموش میگردد. اما دلایل دیگری هم برای وقوع این مشکل وجود دارد. همانند شارژ شدن با سرعت بالا و یا بیش از ظرفیت تعیین شده.
شارژ فراتر از ظرفیت تعیین شده همانند پر کردن بیش از اندازهی یک سطل آب است. طبیعتا مهم نیست که با چه سرعتی سطل در حال پر شدن باشد، اما نهایتا منجر به سرریز شدن میگردد. در باتریها هم هنگامی سرریز رخ میدهد که لیتیوم اضافی وارد آند گردد. این نکته را هم بگوییم که این ریسکی نیست که شما هر شب در اتصال گوشیتان به شارژر انجام میدهید. چرا که اکثر باتریهای امروزی مدارات کنترلی داخلی دارند که به هنگام شارژ کامل، بهطور خودکار باتری را از حالت شارژ خارج میکند. البته مشکلی که در اینجا پیش میآید آن است که امکان بد عمل کردن همین مدار هم وجود دارد. در نتیجه امکان سرریز و در پی آن خرابیهای پس از آن منتفی نیست.
باتری همانند یک نوار الاستیکی است. هنگام شارژ باتری، در حال کشیدن این نوار هستیم. در هنگام استفاده، انگار این نوار کشسان را آرام آرام رها میکنیم. بنابراین اگر بخواهیم بیش از اندازه این نوار کشسان را بکشیم و به دیگر سخن، بیش از اندازه باتری را شارژ کنیم، آنوقت است که وارد مشکل شدهایم.
اما شارژ با سرعت بالا چطور میتواند مشکلساز باشد. هنگام حرکت لیتیومها با سرعت بالا، جایابی مناسب برای قرارگیری دچار اختلال میگردد و بنابراین لیتیومها جایگاه پایداری پیدا نخواهند کرد. در پی این کار، زنجیرهای از لیتیومهای متصل بههمی شکل میگیرد که هیچکدام جایگاه پایداری ندارند و میتوانند منجر به اتصال کوتاه گردند.
آخرین مشکل رایجی که برای باتریها پیش میآید، افزایش ظرفیت باتریها توسط افزایش ولتاژ است. ولتاژ راهی برای اندازهگیری نیرو است. به ولتاژ همانند ارتفاع یک آبشار نگاه کنید و جریان را مقدار آبِ جاری. هر چه ولتاز بالاتر رود، توان بیشتری در باتری موجود خواهد بود. بنابراین سازندگان با افزودن نیکل به لیتیوم سعی میکنند ولتاژ را بالا ببرند. اما همانطور که پیشتر گفته شد، هرچه ولتاژ بالاتر رود، احتمال آنکه الکترولیتها به هم متصل گردند، بیشتر میگردد.
دانشمندان در تلاشند با جایگزین کردن یونلیتیوم با مایع یونیک، مشکلات باتری را مرتفع کنند. اما به گفتهی خودشان، همچنان مشکل راندمان و ظرفیت در مادهی جدید پا برجاست.
برای Galaxy Note 7 نیز چنین اتفاقی افتاده بود. جداکنندهها خراب شده بودند و الکترودها به یکدیگر متصل شده بودند. برای باتری این بدترین اتفاق است، چرا که منجر به انفجار و آتشسوزی میگردد. هنگامی که التکرودها به هم تماس پیدا میکنند، تمامی انرژیها به جای آنکه به دو سمت(قطب) باتری سرازیر شوند، به مرکز باتری که الکترولیتها قرار دارند، میروند.
الکترولیتها خیلی پایدار نیستند و در اثر کوچکترین تغییراتی از حالت ایمن خارج میشوند. هنگامی که گرمای زیاد، چه به دلیل گرمای بیرونی و چه اتصال کوتاه، ایجاد میشود، میتواند الکترولیتها را به واکنش با دیگر مواد شیمیایی و تولید گازهایی وادار کند که همین تولید گاز منجر به گرمای بیشتری گردد. هر بار که این مواد شیمیایی با یکدیگر واکنش انجام میدهند، گازهای بیشتری با سرعت بالاتری تولید میکنند. این کار باعث ورود به حلقهای به نام «گریز گرما» میگردد که نهایتا چیزی جزء آتشسوزی و انفجار نیست. به همین دلیل است که هنگامی که گوشی موبایل بیش از اندازه داغ شد، دستگاه به طور خودکار خاموش میگردد. اما دلایل دیگری هم برای وقوع این مشکل وجود دارد. همانند شارژ شدن با سرعت بالا و یا بیش از ظرفیت تعیین شده.
شارژ فراتر از ظرفیت تعیین شده همانند پر کردن بیش از اندازهی یک سطل آب است. طبیعتا مهم نیست که با چه سرعتی سطل در حال پر شدن باشد، اما نهایتا منجر به سرریز شدن میگردد. در باتریها هم هنگامی سرریز رخ میدهد که لیتیوم اضافی وارد آند گردد. این نکته را هم بگوییم که این ریسکی نیست که شما هر شب در اتصال گوشیتان به شارژر انجام میدهید. چرا که اکثر باتریهای امروزی مدارات کنترلی داخلی دارند که به هنگام شارژ کامل، بهطور خودکار باتری را از حالت شارژ خارج میکند. البته مشکلی که در اینجا پیش میآید آن است که امکان بد عمل کردن همین مدار هم وجود دارد. در نتیجه امکان سرریز و در پی آن خرابیهای پس از آن منتفی نیست.
باتری همانند یک نوار الاستیکی است. هنگام شارژ باتری، در حال کشیدن این نوار هستیم. در هنگام استفاده، انگار این نوار کشسان را آرام آرام رها میکنیم. بنابراین اگر بخواهیم بیش از اندازه این نوار کشسان را بکشیم و به دیگر سخن، بیش از اندازه باتری را شارژ کنیم، آنوقت است که وارد مشکل شدهایم.
اما شارژ با سرعت بالا چطور میتواند مشکلساز باشد. هنگام حرکت لیتیومها با سرعت بالا، جایابی مناسب برای قرارگیری دچار اختلال میگردد و بنابراین لیتیومها جایگاه پایداری پیدا نخواهند کرد. در پی این کار، زنجیرهای از لیتیومهای متصل بههمی شکل میگیرد که هیچکدام جایگاه پایداری ندارند و میتوانند منجر به اتصال کوتاه گردند.
آخرین مشکل رایجی که برای باتریها پیش میآید، افزایش ظرفیت باتریها توسط افزایش ولتاژ است. ولتاژ راهی برای اندازهگیری نیرو است. به ولتاژ همانند ارتفاع یک آبشار نگاه کنید و جریان را مقدار آبِ جاری. هر چه ولتاز بالاتر رود، توان بیشتری در باتری موجود خواهد بود. بنابراین سازندگان با افزودن نیکل به لیتیوم سعی میکنند ولتاژ را بالا ببرند. اما همانطور که پیشتر گفته شد، هرچه ولتاژ بالاتر رود، احتمال آنکه الکترولیتها به هم متصل گردند، بیشتر میگردد.
دانشمندان در تلاشند با جایگزین کردن یونلیتیوم با مایع یونیک، مشکلات باتری را مرتفع کنند. اما به گفتهی خودشان، همچنان مشکل راندمان و ظرفیت در مادهی جدید پا برجاست.

 هک کردن راحت بازی های اندروید با برنامه GameCih
هک کردن راحت بازی های اندروید با برنامه GameCih آموزش ساخت پهباد کوچک در خانه!!
آموزش ساخت پهباد کوچک در خانه!! Apple سری جدید Mac خود را در ۲۷ اکتبر معرفی خواهد کرد
Apple سری جدید Mac خود را در ۲۷ اکتبر معرفی خواهد کرد 10 شغل تکنولوژی مربوط به آینده که باور نخواهید کرد که واقعا وجود دارند
10 شغل تکنولوژی مربوط به آینده که باور نخواهید کرد که واقعا وجود دارند 950 میلیون دستگاه اندرویدی در خطر هک شدن از طریق پیام رسانی
950 میلیون دستگاه اندرویدی در خطر هک شدن از طریق پیام رسانی دانشمندان تراشه ای اختراع کرده اند که می تواند پرواز سوسک ها را در کنترل بگیرد
دانشمندان تراشه ای اختراع کرده اند که می تواند پرواز سوسک ها را در کنترل بگیرد اوج خلاقیت در چهارمین نمایشگاه پرینترهای سه بعدی
اوج خلاقیت در چهارمین نمایشگاه پرینترهای سه بعدی سوپر ربات چینی به راحتی با مردم ارتباط برقرار می کند
سوپر ربات چینی به راحتی با مردم ارتباط برقرار می کند گوگل در پی کشف هیولای افسانه ای
گوگل در پی کشف هیولای افسانه ای اشک شوق: چاپگر 3D به مادر نابینا امکان داد تا پسر خود را ‘ببیند’
اشک شوق: چاپگر 3D به مادر نابینا امکان داد تا پسر خود را ‘ببیند’


